- Пероксид натрия
-
Пероксид натрия 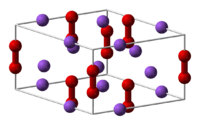
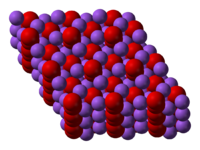
Общие Систематическое наименование пероксид натрия Химическая формула Na2O2 Физические свойства Состояние (ст. усл.) желтоватый порошок Отн. молек. масса 78 а. е. м. Молярная масса 78 г/моль Плотность 2.8 г/см³ Термические свойства Температура плавления 675 °C Энтальпия образования (ст. усл.) -513 кДж/моль Химические свойства Растворимость в воде реагирует Классификация Рег. номер CAS [1313-60-6] Пероксид натрия (перекись натрия), Na2O2 — желтовато-белые кристаллы с ионной кристаллической решеткой.
Содержание
Свойства
Энергично реагируют с водой со значительным выделением тепла:
Для пероксида натрия характерно образование хорошо кристаллизующихся гидратов и аддуктов с пероксидом водорода. Так, быстрой кристаллизацией пероксида натрия из ледяной воды легко осаждается гидрат Na2O2•8H2O.
Пероксид натрия является сильным оксилителем. С восстановителями, такими, как сера, порошок алюминия, эфиры реагирует с образованием пламени. С монооксидом углерода реагирует менее активно, образуя карбонат:
Окисление аммиака пероксидом натрия приводит к образованию нитрата натрия:
Получение
Пероксид натрия образуется при сгорании натрия в кислороде:
Применение
Применяют для отбеливания тканей, шерсти, шелка, древесной и вискозной массы, соломы. Для получения кислорода, поглощения угарного и углекислого газа используется в регенерационных установках и изолирующих противогазах:
Литература
- Кнунянц И. Л. и др. т.3 Мед-Пол // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1992. — 639 с. — 50 000 экз. — ISBN 5-85270-039-8

Для улучшения этой статьи желательно?: - Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
Категории:- Соединения натрия
- Пероксиды
- Неорганические вещества
-
Wikimedia Foundation. 2010.





