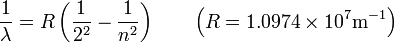Формула Бальмера-Ридберга
- Формула Бальмера-Ридберга
-
Серия Бальмера — спектральная серия в спектре атома водорода, названная в честь швейцарского физика Иоганна Бальмера, открывшего эту серию в 1885 году. Данная серия образуется при переходах электронов с возбужденных энергетических уровней на второй в спектре излучения и со второго уровня на все вышележащие уровни при поглощении. Переход с третьего энергетического уровня на второй обозначается греческой буквой α, с 4-го на 2-й — β и т. д. Для обозначения самой серии используется латинская буква H. Таким образом, полное обозначение спектральной линии, возникающей при переходе электрона со третьего уровня на второй — Hα (произносится Бальмер альфа).
Серия Бальмера
Формула Ридберга для серии Бальмера выглядит следующим образом:
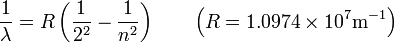
Где n — главное квантовое число — натуральное число большее 2.
Первые 4 линии серии находятся в видимом диапазоне, остальные — в ультрафиолетовом:
| Обозначение |
Hα |
Hβ |
Hγ |
Hδ |
Hε |
Hζ |
Hη |
Граница серии |
| Длина волны, нм |
656.3 |
486.1 |
434.1 |
410.2 |
397.0 |
388.9 |
383.5 |
364.6 |
См. также
Ссылки
Wikimedia Foundation.
2010.
Полезное
Смотреть что такое "Формула Бальмера-Ридберга" в других словарях:
Формула Ридберга — в том виде, в котором она была представлена в ноябре 1888 года Формула Ридберга эмпирическая формула, описывающая длины волн в спектрах излучения атомов химических элементов. Предложена шведским учёным Йоханнесом Ридбергом и предста … Википедия
Серия Бальмера — Серия Бальмера спектральная серия, наблюдающаяся для атомов водорода[1]. Названа в честь швейцарского физика Иоганна Бальмера, описавшего в 1885 году эту серию формулой (см. ниже Формула Бальмера). Содержание 1 … Википедия
Серия Пашена — (Серия Ритца Пашена) спектральная серия в спектре атома водорода, названная в честь австрийского физика Фридриха Пашена, открывшего в 1908 году эту серию, ранее предсказанную Вальтером Ритцем на основании его комбинационного принципа … Википедия
Серия Лаймана — Серия Лаймана спектральная серия в спектре атома водорода, названная в честь американского физика Теодора Лаймана, открывшего эту серию в … Википедия
Серия Хэмпфри — Серия Хэмпфри спектральная серия в спектре атома водорода, названная в честь американского физика Кёртиса Хэмпфри, открывшего эту серию в 1953 году. Данная серия образуется при переходах электронов с возбуждённых энергетических уровней на… … Википедия
Серия Брэккета — Серия Брэккета спектральная серия в спектре атома водорода, названная в честь американского физика Фредерика Брэккета, открывшего эту серию в 1922 году. Данная серия образуется при переходах электронов с возбужденных энергетических уровней… … Википедия
Серия Пфунда — Серия Пфунда спектральная серия в спектре атома водорода, названная в честь американского физика Августа Пфунда, открывшего эту серию в 1924 году. Данная серия образуется при переходах электронов с возбужденных энергетических уровней на… … Википедия
Постулаты Бора — Постулаты Бора основные допущения, сформулированные Нильсом Бором в 1913 году для объяснения закономерности линейчатого спектра атома водорода и водородоподобных ионов (формула Бальмера Ридберга) и квантового характера испускания и… … Википедия
Бора постулаты — Постулаты Бора основные допущения, сформулированные Нильсом Бором в 1913 году для объяснения закономерности линейчатого спектра атома водорода (формула Бальмера Ридберга), ядерной модели атома и квантового характера испускания и поглощения света … Википедия
Спектральные серии водорода — Спектральные серии водорода набор спектральных серий, составляющих спектр атома водорода. Поскольку водород наиболее простой атом, его спектральные серии наиболее изучены. Они хорошо подчиняются формуле Ридберга: , где R = 109 677… … Википедия