- Трифторид азота
-
Трифторид азота 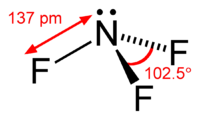

Общие Систематическое наименование Трифторид азота Химическая формула NF3 Отн. молек. масса 71,0019 а. е. м. Молярная масса 71,0019 г/моль Физические свойства Плотность вещества 3,003 кг/м³ (газ, 15 °C); 1,540 (жидкий при температуре кипения) г/см³ Состояние (ст. усл.) бесцветный газ Термические свойства Температура плавления −206,79 °C Температура кипения −129,01 °C Химические свойства Растворимость в воде 0,021 г/100 мл Классификация номер CAS [7783-54-2]
Трифтори́д азо́та (фторид азота(III), трёхфтористый азот) — NF3, фторсодержащий аналог аммиака, в котором атомы водорода замещены атомами фтора. Бесцветный ядовитый тяжёлый газ. Негорюч, вызывает коррозию металлов. Имеет характерный запах плесени. Слегка растворим в воде.Содержание
Открытие
Трёхфтористый азот был впервые получен Руффом, Фишером, Люфтом в 1928 путем электролиза раствора фторида аммония в фтороводороде.
Физические свойства
- Температура критическая: −39,26 °C
- Критическое давление: 44,72 атм.
- Плотность: 1,54 г/см³ (жидкость, -129 °C)
- Плотность критическая:
- Теплота образования: −30,4 ккал/моль
Химические свойства
Получение
Промышленным методом получения является паровая конверсия фторо-аммиачных газовых смесей. Мировой объём производства оценивается в 100 т. на 1992 год и в 4000 т. на 2007 год; предполагается, что он увеличится до 8000 т. к 2011 году.
Применение
Применяется для изготовления ЖК мониторов, тонкопленочных солнечных батарей и микросхем.
Токсичность
Экологичность
Трифторид азота по своим свойствам является парниковым газом и провоцирует глобальное потепление (по оценкам, в 17 200 раз активнее, чем углекислый газ той же массы при действии в течение 100 лет)[1][2][3]. Согласно исследованиям, количество NF3 в атмосфере равно 5400 т. в 2008 г. и повышается на 11% каждый год, причём его среднее время жизни в атмосфере составляет от 550 до 740 лет.
Литература
- С.Сарнер. Химия ракетных топлив. М.: «Мир», 1969.
- Schmidt E. W., Harper J. T., Handling and Use of Fluoride and Fluorine-Oxygen Mixtures in Rocket Systems, Lewis Research Center, NASA SP-3037, Cleveland, Ohio, 1967.
- пресс-релиз НАСА и популярная заметка в Компьюленте.
- ↑ Climate Change 2007: The Physical Sciences Basis, IPCC, <http://www.ipcc.ch/pdf/assessment-report/ar4/wg1/ar4-wg1-chapter2.pdf>. Retrieved on 2008-07-03.06.2009
- ↑ Robson, J.I.; Gohar, L.K., Hurley, M.D., Shine, K.P. and Wallington, T. (2006). "Revised IR spectrum, radiative efficiency and global warming potential of nitrogen trifluoride". Geophys. Res. Lett. 33. DOI:10.1029/2006GL026210.
- ↑ Richard Morgan. Beyond Carbon: Scientists Worry About Nitrogen’s Effects, New York Times (2008-09-01). Проверено 2008-09-07. mirror
Wikimedia Foundation. 2010.
