- Глутатионпероксидазы
-
Глутатинопероксидаза 1
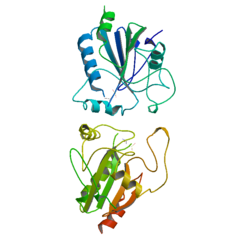
Обозначения Символы Entrez Gene HGNC OMIM RefSeq UniProt Другие данные Шифр КФ Локус 3-я хр., глутатионпероксидаза 3 (содержится в плазме крови)Обозначения Символы Entrez Gene HGNC OMIM RefSeq UniProt Другие данные Шифр КФ Локус 5-я хр., глутатионпероксидаза 5 (эпидермальный, андрогенсвязанный белок)Обозначения Символы Entrez Gene HGNC OMIM RefSeq UniProt Другие данные Шифр КФ Локус 6-я хр., глутатионпероксидаза 6 (зрительная система)Обозначения Символы Entrez Gene HGNC OMIM RefSeq UniProt Другие данные Шифр КФ Локус 6-я хр., Глутатионпероксидазы (ГП, англ. Glutathione peroxidase, PDB 1GP1, (КФ 1.11.1.9) — семейство ферментов, защищающих организм от окислительного повреждения. Глутатионпероксидазы катализируют восстановление перекисей липидов в соответствующие спирты и восстановление пероксида водорода до воды. Известно несколько генов, кодирующих разные формы глутатионпероксидаз, отличающиеся по локализации в организме. Структурно ферменты данного семейства представляют собой селеносодержащие тетрамерные гликопротеины.
Содержание
Изоферменты
Существует несколько изоферментов, которые кодируются разными генами. Изоферменты отличаются по локализации в клетке и субстратной специфичности. Глутатионпероксидаза 1 (GPx1) является наиболее распространенной формой фермента, и обнаружена в цитоплазме практически всех тканей млекопитающих, субстратом GPx1 является пероксид водорода. Глутатионпероксидаза 4 (GPx4) имеет большое значение в метаболизме пероксдов липидов; GPx4 также экспрессируется практически во всех клетках млекопитающих на более низких уровнях. Глутатионпероксидаза 2 (GPx2) экспрессируется в кишечнике и является внеклеточным ферментом, GPx3 также является внеклеточным ферментом и в основном встречается в плазме.[1] У человека были идентифицированы восемь изоформ глутатионпероксидазы.
Глутатионпероксидаза, выделенная из эритроцитов быка имеет молекулярную массу около 84 кДа.
Реакция
Примером реакции, катализируемой ферментом глутатионпероксидазой является реакция:
2GSH + H2O2 → GS-SG + 2H2O.где
GSHобозначает восстановленный мономерный глутатион, аGS-SG— дисульфид глутатиона.Фермент глутатионредуктаза далее восстанавливает окисленный глутатион и завершает цикл:
GS-SG + NADPH + H+ → 2 GSH + NADP+.Структура
Обнаружено, что относящиеся к млекопитающим GPx1, GPx2, GPx3 и GPx4 являются селеносодержащими ферментами, тогда как GPx6 — селенопротеин человека с цистеин-содержащими гомологами у грызунов. GPx1, GPx2 и GPx3 являются гомотетрамерными белками, тогда как GPx4 имеет a мономерную структуру. Поскольку целостность клеточных и внутриклеточных мембран сильно зависит от глутатионпероксидазы, антиоксидантные защитные системы самой глутатионпероксидазы сильно зависят от наличия селена.
Механизм реакции
В активном центре фермента находится остаток аминокислоты селеноцистеина. Атом селена находится в степени окисления −1 и окисляется пероксидом до SeOH. Далее SeOH соединяется с молекулой глутатиона (GSH), образуя Se-SG и далее соединяется с другой молекулой глутатиона. При этом регенерируется Se− и образуется побочный продукт GS-SG.
Нокауты генов
Мыши, нокаутные по гену Gpx1 глутатитонпероксидазы имеют нормальный фенотип, нормальную продолжительность жизни. Эти данные указывают на то, что данный фермент не является критичным для жизнедеятельности. Однако, у мышей, нокаутных по двум копиям гена, преждевремнно развивается катаракта и наблюдаются дефекты в пролиферации вспомогательных мышечных клеток.[1] Однако, мыши нокаутные по гену GPX4 глутатионпероксидазы 4, погибают в течение раннего эмбрионального развития.[1] Существуют данные, свидетельствующие о том, что пониженный уровень глутатионпероксидазы 4 может повышать продолжительность жизни у мышей.[2]
Данные о нокаутах других генов, кодирующих глутатионпероксидазы, отсутствуют.
Открытие
Глутатионпероксидаза была открыта в 1957 году Гордоном Миллсом.[3]
Примечания
- ↑ 1 2 3 Muller FL, Lustgarten MS, Jang Y, Richardson A, Van Remmen H (August 2007). «Trends in oxidative aging theories». Free Radic. Biol. Med. 43 (4): 477–503. DOI:10.1016/j.freeradbiomed.2007.03.034. PMID 17640558.
- ↑ Ran Q, Liang H, Ikeno Y, et al. (2007). «Reduction in glutathione peroxidase 4 increases life span through increased sensitivity to apoptosis». J. Gerontol. A Biol. Sci. Med. Sci. 62 (9): 932–42. PMID 17895430.
- ↑ MILLS GC (November 1957). «Hemoglobin catabolism. I. Glutathione peroxidase, an erythrocyte enzyme which protects hemoglobin from oxidative breakdown». J. Biol. Chem. 229 (1): 189–97. PMID 13491573.
См. также

Оксидоредуктазы: пероксидазы (КФ 1.11) 1.11.1.1-14 Каталаза - Цитохромпероксидаза - Пероксидаза эозинофилов - Глутатионпероксидаза - Пероксидаза хрена - Лактопероксидаза - Миелопероксидаза - Тиреопероксидаза - Дейодиназа (Т4-5'-дейодиназа) 1.11.1.15 (пероксиредоксин) 1 - 2 - 3 - 4 - 5 - 6 Категории:- Гены 3-й хромосомы
- Гены 5-й хромосомы
- Гены 6-й хромосомы
- Ферменты
- Антиоксиданты
Wikimedia Foundation. 2010.